Gynäkologie - Gutartige Erkrankungen - Infektionen & Dermatosen
Aerobe Vaginitis/Desquamative entzündliche Vaginitis:
Es handelt sich um eine Entzündung der Scheide, welche vermutlich immunologisch induziert ist. Leitsymptome dieser Scheideninfektion sind brennende Schmerzen,
fleckförmige Rötung der Scheidenhaut (Erythem) und
gelbgrüner dünner Ausfluss. Der pH-Wert ist stark erhöht. In der Phasenkontrastmikroskopie sieht man
mehr als 100 weiße Blutkörperchen (Leukozyten) im Gesichtsfeld bei 400-facher Vergrößerung (oft "toxisch" verändert, nämlich rundlich ohne strukturierten Inhalt, ohne gelappten Zellkern), auch Plasmazellen und nur wenige kokkoide Erreger. Bei schweren Fällen treten auch
Parabasalzellen auf. Heilung erreicht man in leichten unkomplizierten Fällen durch einwöchige lokale Therapie mit Clindamycin. Bleibt der Erfolg aus oder treten Rezidive auf, sollte die örtliche Behandlung bis zu vier Wochen fortgeführt werden oder Clindamycin in Tablettenform über 10 Tage (4x 300 mg/Tag) eingesetzt werden. Clindamycin verhindert die Synthese von proinflammatorischen Zytokinen ähnlich wie Cortsion. Alternativ kann eine Vaginalcreme aus 0,15 % Estradiolvalerat, 0,3 % Clindamycin und 0,5 % Hydrocortison (Apothekenherstellung, ad 40,0 Basiscreme DAC) eingesetzt werden, die ein- bis dreimal wöchentlich (2 g) in die Scheide für die Dauer von 4 Monaten appliziert wird.
Atopisches Ekzem/Neurodermitis:
Ein atopisches Ekzem beruht auf einer anlagebedingten Überempfindlichkeit der Haut mit Neigung zur Ekzembildung. Die Vulva kann singulär betroffen sein, begleitet von Juckreiz und chronischem Verlauf. Morphologisch findet man unscharf begrenzte Erytheme an den großen und kleinen Schamlippen sowie Ödembildung im akuten Stadium und Lichenifikation (Verdickung der Haut, Vergröberung der Hautstruktur, Verminderung der Hautgeschmeidigkeit, Vertiefung der Hautfurchen) im chronischen Stadium. Das Ekzem entsteht auf der Basis eines gestörten epidermalen Lipoidstoffwechsels. Dies führt zu Schäden der Hautbarriere und damit zur ständigen Anregung von entzündlichen Reaktionen der Epidermis. Toxische Stimula wie lokale Medikamente und Kosmetika verschärfen die Situation. Insbesondere antientzündlich wirkende Antimykotika können Besserung vortäuschen, da diese vorübergehend den Juckreiz nehmen. Eine regelrecht toxische Wirkung für die Haut mit gestörter Barrierefunktion geht von Milchsäurebakterien aus.
Die Diagnose atopische Dermatitis kann ohne Biopsie auskommen, wenn drei der vier folgenden Basissymptome vorliegen:
- Juckreiz
- Ekzembildung im Bereich der Vulva und anderen charakteristischen Arealen (Beugenbetonung bei Erwachsenen)
- Chronisch rezidivierender Verlauf
- Positive Eigen- und Familienanamnese
Die Therapie basiert auf folgenden Grundsätzen:
- Basispflege mit rückfettenden Cremes
- Antientzündliche Therapie
- Vermeidung von Provokationsfaktoren
Pflegende Basistherapeutika sind Produkte wie Deumavan®, Dexeryl® und Neuroderm® Pfegeecreme. Letztere enthält mit 20 % Glycerin einen natürlichen Feuchthaltefaktor. Dieser bewirkt eine Erhöhung der Hautfeuchtigkeit. Der Lipidanteil von 30 % sorgt für eine gute Rückfettung der Haut. Dadurch wird die Barriere-Funktion der Haut erheblich verbessert.
Für die antientzündliche Therapie des Vulvaekzems sind Glukokortikoide der unteren Wirkklassen wie Prednicarbat (Dermatop®) oder Methylprednisolon-Aceponat (Advantan®) ausreichend. Sie sollten anfangs 2x täglich angewandt werden, jedoch nicht länger als 4 Wochen. Danach sollte ein Wechsel zu kortisonfreien antientzündlichen Ersatzstoffen erfolgen, die auch bei längerfristiger Anwendung nicht zur Hautatrophie führen. Bewährt haben sich hierbei die Immunmodulatoren Tacrolismus (Protopic®) und Pimecrolismus (Elidel®), die 2x tgl. solange angewandt werden, bis keine Symptome mehr bestehen. Um Ekzemschübe dauerhaft zu vermeiden, wird eine bis zu zwölf Monate dauernde Erhaltungstherapie (Protopic®) empfohlen, 2x wöchentlich. Vor allem zu Behandlungsbeginn wird Tacrolimus allerdings lokal schlecht vertragen: Mit Brennen der Haut (50 %), Pruritus (25 % bis 50 %) und Hautrötung (über 10 %) ist zu rechnen. Bei 1 % bis 10 % der Anwender kommt es zu Akne, Hyperästhesie und Alkoholunverträglichkeit (Rötung der Gesichtshaut oder Hautreizungen nach Alkoholgenuss). Der Gebrauch des Externums geht häufig mit infektiösen Folgen einher wie Follikulitis (7 % bis 8 % der Erwachsenen) und Herpes simplex einschließlich Eczema herpeticum (1 % bis 10 %). Die Basistherapie mit rückfettender Basiscreme bleibt während der gesamten Behandlungszeit bestehen und sollte auch darüber hinaus fortgesetzt werden.
Zu den wichtigsten lokalen Provokationsfaktoren zählen Antiinfektiva und deren Begleitstoffe. Ein trockenes Milieu durch exzessive Anwendung von Tampons sollte vermieden werden. Auch psychische Belastungen können Schübe auslösen.
Bakterielle Vaginose:
Als bakterielle Vaginose wird eine krankhafte Veränderung des Scheidenmilieus bezeichnet. Sie ist die häufigste Störung der Scheidenflora durch Bakterien, ist aber keine Geschlechtskrankheit. Allerdings kann Geschlechtsverkehr das Risiko für das Auftreten einer bakteriellen Vaginose erhöhen. Man schätzt, dass ca. 5.000 von 100.000 Frauen im Jahr von einer solchen Veränderung des Scheidenmilieus betroffen sind. Innerhalb von 7 Tagen nach Kontakt mit auslösenden Erregern kommt es in der Regel zu Beschwerden.
Als besondere Risikofaktoren gelten im Zusammenspiel mit einer genetischen Disposition:
- Oralsex am weiblichen Genitale
- die vaginale Penetration mit dem Finger
- Analverkehr vor vaginalem Sex, wenn keine Kondome verwendet werden
Ist die Scheidenflora gesund, findet man hauptsächlich Milchsäurebakterien (Laktobazillen, Lactobacillus) vor. Dominierende Laktobazillen sind L. crispatus, L. gasseri, L. jensenii, L. acidophilus und L. iners. Die meisten Laktobazillen sorgen für ein saures Scheidenmilieu, indem sie Milchsäure und Wasserstoffperoxid produzieren. Das saure Milieu bildet eine Art natürlichen Schutzschild und schützt die Scheidenflora vor einer Besiedlung durch andere Keime. Lediglich Lactobacillus iners ist nicht in der Lage zur Produktion von Milchsäure und Wasserstoffperoxid.
Ist die Scheidenflora aus dem Gleichgewicht geraten, dann ist es zu Besiedelungen durch Bakterien oder Pilze gekommen, welche die Milchsäurebakterien verdrängt haben. Bei einer bakteriellen Vaginose findet man dann vor allem große Mengen an Gardnerella-Bakterien (Gardnerella vaginalis) in der Scheidenflora vor sowie in unterschiedlichem Ausmaß andere unter Luftausschluss (anaerob) lebende Bakterienarten wie
Atopobium vaginae, welches sich mikroskopisch nicht von den Laktobazillen unterscheidet, und auch vielleicht noch sehr kleine Bakterien ohne Zellwand namens Mykoplasmen.
Etwa 50 Prozent der Patientinnen klagen typischerweise über
grau-weißen Ausfluss, der vermehrt, cremig, schaumig oder dünnflüssig sein kann. Dem Ausfluss haftet ein unangenehmer, meist fischiger Geruch an, der durch die gebildeten Amine entsteht.
Im äußeren Scheidenbereich können Juckreiz und Hautreizungen auftreten. Auch werden gelegentlich Schmerzen beim Geschlechtsverkehr oder Wasserlassen festgestellt. Bei der bakteriellen Vaginose liegt keine Entzündung der Scheide vor.
Die bakterielle Vaginose gilt nicht nur als ästhetisches Problem, sie erhöht gleichzeitig das Risiko für gynäkologische Infektionen des Inneren Genitale (Gebärmutter, Eileiter, Eierstöcke) in besonderem Maße.
Die Behandlung erfolgt über Gabe von Antibiotika wie
Metronidazol, Clindamycin oder lokalen Antiseptika wie Dequaliniumchlorid (Fluomizin®) oder Octenidin (octenisept® Vaginaltherapeutikum) in Form von Tabletten, Scheidenzäpfchen, Scheidencreme oder Vaginallösung. Diese Medikamente töten die anaeroben Keime in der Vagina. Dabei gelten Metronidazol und Clindamycin als Mittel der Wahl. Die Dauer und Intensität der Behandlung richtet sich nach der Schwere der Erkrankung, der Regenerationsfähigkeit der Vaginalflora sowie etwaiger Begleitumstände. Besonders die beiden Leitkeime Atopium vaginae und G. vaginalis können einen Biofilm formen, in den Antibiotika nicht tief eindringen können, wodurch es nach wenigen Monaten zu Rezidiven kommen kann. Unter Therapie mit Metronidazol sollte aufgrund des sogenannten Disulfiram-Effektes Alkoholgenuss vermieden werden. Die vaginalen Applikationsformen von Metronidazol und Clindamycin können das Material von Kondomen angreifen und damit die Verhütungsmethode unsicher machen. Zu beachten ist, dass Atopobium vaginae resistent auf eine Behandlung mit Metronidazol ist. Antibiotikum der Wahl bei diesem Keim ist Clindamycin.
Wird die bakterielle Vaginose mit Antibiotika behandelt,
heilt sie
in der Regel innerhalb weniger Tage ab . Allerdings kommt es häufig zu Rückfällen.
Auch Lactobacilluspräparate, Milchsäure oder Ascorbinsäure (Vitamin C) zur Ansäuerung bzw. Wiederaufbau des natürlichen Scheidenmilieus können Wirkung zeigen und werden auch zur Vorbeugung von Rezidiven eingesetzt.
Studien zeigen, dass bei betroffenen Frauen meist auch beim Sexualpartner Gardnerella-Bakterien nachweisbar sind. Bei Männern führt dies jedoch in der Regel nicht zu Beschwerden. Um die Rückfallhäufigkeit bei immer wieder kehrenden Vaginosen zu senken, ist eine Mitbehandlung des Partners in solchen Fällen durchaus sinnvoll.
Chronisch rezidivierende bakterielle Vaginosen können beispielsweise nach folgendem Schema behandelt werden:
- Sobelin® Kapseln: Beide Partner synchron 2x 300 mg täglich über 4 Tage. Clindamycin behandelt Gardnerella vaginalis und Begleitkeime wie Atopobium vaginae. Gesunde E. coli-Keime im Darm bleiben von Clindamycin dagegen verschont
- Sobelin Vaginalcreme: Morgens und abends maximal tief intravaginal einführen, die Schamlippen behandeln, auch unter der Vorhaut und um die Klitoris
- Arilin-Zäpfchen: jeweils ein Zäpfchen tief vaginal vor der Nacht über 6 Tage
- Wiederaufbau der Vaginalflora mit z. B. Vagisan ProbioFlora® Milchsäure-Bakterien (8 Tage abends vor dem Schlafengehen je eine Vaginalkapsel) oder OMNi-BiOTiC® FLORA plus+ 1-2 x täglich ein Beutel (in ca. 1/8 l Wasser einrühren, mindestens 1 Minute Aktivierungszeit abwarten, nochmals umrühren und dann trinken)
Eine Alternative stellt die topische Behandlung mit Antiseptika oder eine suppressive Erhaltungstherapie mit Metronidazol 2x wöchentlich für insgesamt 16 Wochen dar, gefolgt von vaginalen Probiotika. Eine Partnertherapie kann ebenfalls in Betracht gezogen werden.
Eine Bartholinitis stellt eine Entzündung einer der großen Scheidenvorhofdrüsen, Bartholin-Drüsen genannt, dar. Diese Drüsen sind für die Aussonderung von Sekreten in die Scheide für das Befeuchten des Scheideneinganges zuständig. Wird die Sekretion solch einer Drüse durch einen Verschluss des Ausganges gehindert, so staut sich das Sekret und es entsteht eine Bartholin-Zyste. Eine Schwellung im unteren Bereich der großen Schamlippe, eventuell Rötung und Schmerzen sind die Folge. Die häufigsten Verursacher sind Bakterien. Sie gelangen über den Scheideneingang in die Drüse und verursachen dort die Entzündung. Häufig sind verschiedene sogenannte anaerobe Keime ursächlich. Im Frühstadium können Sitzbäder mit desinfizierenden Zusätzen das Abklingen der Zyste bewirken. Führt dies nach 3-4 Tagen nicht zum Erfolg oder ist die Entzündung schmerzhaft, müssen Antibiotika, z. B. Metronidazol und Doxycyclin, und ggf. Antiphlogistika eingesetzt werden. Bei einem ausgeprägten Lokalbefund bleibt eine chirurgische Methode, die sogenannte Marsupialisation, als letzte Alternative übrig. Unter Narkose wird durch Einschneiden der Zyste das Ausfließen des Eiters hervorgerufen und anschließend wird die Zystenwand nach außen mit der Umgebung vernäht. Dadurch bleibt die Zyste offen und kann austrocknen.
Das Behcet-Syndrom ist eine Dermatose, hervorgerufen durch eine Entzündung von Gefäßen. Das Syndrom wird dem Rheumatischen Formenkreis zugeordnet. Die Entzündung führt zur Entwicklung von kleinen Geschwüren bevorzugt an der Innenseite der kleinen Schamlippen. Gleichzeitig können sich sogenannte Aphthen an der Mundschleimhaut entwickeln. Die Erkrankung tritt akut und schmerzhaft auf. Zur Unterscheidung zum primären Herpes genitalis sind die Leistenlymphknoten nicht geschwollen. Die Diagnose wird allein aus dem klinischen Bild und dem Verlauf beziehungsweise der raschen Abheilung durch eine Kortikosteroidsalbe gestellt. Ohne Behandlung verläuft der Heilungsprozess sehr langsam über 4-8 Wochen.
Chlamydien:
Warum sollte man sich über Chlamydieninfektionen informieren?
- Chlamydien verursachen zu Beginn der Infektion keine oder nur geringe Beschwerden.
- Chlamydieninfektionen sind im Frühstadium gut zu behandeln.
- Chlamydien können zur Unfruchtbarkeit führen.
- Chlamydien können ohne Behandlung zu chronischen Beschwerden führen.
- Folgen einer Chlamydieninfektion sind nicht mehr oder kaum noch zu beseitigen, wenn die Infektion zu spät erkannt wird.
Chlamydien gehören zu den kleinsten Bakterien und sind sehr schwer nachweisbar. Es gibt eine ganze Reihe von Chlamydienarten, die beim Menschen und beim Tier verschiedenste Krankheiten auslösen können. Die im Hinblick auf eine Infektion des Urogenitalbereichs bedeutsame Chlamydienart heißt Chlamydia trachomatis. Sie wird
von Mensch zu Mensch über direkten Kontakt, meist über den Geschlechtsverkehr übertragen . Da alle Erreger, die im Genitalbereich vorhanden sind, bei der Geburt auch auf das Kind übertragen werden können, ist auch die Infektion eines Neugeborenen mit Chlamydien möglich. Neben dem Urogenitaltrakt infizieren die Erreger in Abhängigkeit mit den ausgeübten Sexualpraktiken unter Umständen auch den Enddarm und den Rachen.
Wie häufig sind Chlamydien?
Eine Infektion mit Chlamydia trachomatis gilt neben den humanen Papillomaviren als häufigste sexuell übertragene Krankheit . Sie tritt altersabhängig unterschiedlich häufig auf. Bei über 45-jährigen sind Genitalinfektionen mit Chlamydien nur äußerst selten nachzuweisen, besonders betroffen sind junge, sexuell aktive Menschen nach einem Partnerwechsel. Jugendlichkeit ist deshalb ein Risikofaktor, weil aufgrund der Östrogendominanz in den ersten fertilen Jahren der Gebärmutterhals für Mikroorganismen leicht passierbar ist, die Reifung der lokalen Immunabwehr im Genitaltrakt zunächst noch unvollständig und bei rauchenden Frauen ohnehin vermindert ist.
Schätzungsweise sind chlamydieninfiziert, ohne es zu wissen:
- 6 von 100 Frauen und Männern im Alter von 15-25 Jahren,
- 2 von 100 Frauen und Männern im Alter von 25-45 Jahren,
- 2 von 100 Schwangeren.
Bei Patientinnen mit Gebärmutter- oder Eileiterentzündung sind Chlamydien mehr als 10mal häufiger nachweisbar. Liegt bei Frauen eine Chlamydieninfektion vor, so lässt sich der Erreger bei der Hälfte der Partner ebenfalls nachweisen, wobei der Nachweis auch von der Empfindlichkeit der Testmethode abhängt. Es wird geschätzt, dass in Deutschland ca.
300.000 Frauen pro Jahr neu infiziert werden.
Wie verläuft eine Chlamydieninfektion?
Chlamydien vermehren sich im Vergleich zu den üblichen Bakterien anders und sehr langsam. Das bedeutet, dass auch die Infektion sehr langsam, über Wochen, Monate und Jahre verläuft. Sie beginnt am Muttermund, Mastdarm oder in der Harnröhre und breitet sich bei jedem zweiten Infizierten langsam im Körper aus. Die ersten Beschwerden treten frühestens nach einigen Wochen auf. In dieser Zeit sind die Chlamydien mittels Abstrich vom Muttermund oder aus dem Urin am besten nachweisbar. Nach einiger Zeit befinden sich die Chlamydien in Körperteilen wie Eileitern, Nebenhoden oder Gelenkknorpeln. Ein Nachweis gelingt dann oft nicht mehr so einfach. Der Nachweis der Infektion erlaubt keine Rückschlüsse, wie lange jemand schon infiziert ist und bedeutet daher nicht unbedingt, dass ein Partner fremdgegangen ist.
Woran kann man eine Chlamydieninfektion erkennen?
Oft überhaupt nicht, da Chlamydieninfektionen häufig - insbesondere zu Beginn der Infektion - keine Beschwerden verursachen. Die auftretenden Beschwerden sind meist leichter Natur und sowohl in ihrer Ausprägung als auch ihrer Art wechselnd.
Folgende Krankheitszeichen sollten bei der Frau an eine Chlamydieninfektion denken lassen:
- Brennen beim Wasserlassen, insbesondere wenn keine Blasenentzündung vorliegt,
- Blutungsstörungen, besonders wenn sie unter der Pille oder nach dem Geschlechtsverkehr neu auftreten,
- Ausfluss, besonders gelb und klebrig,
- Bauchschmerzen, die leicht und wechselnd sind,
Schmerzen in der rechten Schulter und Gelenkschmerzen.
Beim Mann können die ersten Anzeichen sein:
- Schmerzen beim Wasserlassen,
- Harndrang und gelber klebriger Ausfluss aus der Harnröhre.
Welches sind die Folgen einer Chlamydieninfektion?
Eine abgelaufene Eileiterentzündung durch Chlamydien gilt als Hauptverursacher infektionsbedingter Sterilität . Die Anzahl der Paare, bei denen in Deutschland eine Unfruchtbarkeit auf eine Chlamydieninfektion zurückzuführen ist, wird auf weit über 100.000 geschätzt.
Ernsthafte Komplikationen bei Frauen sind dementsprechend:
- Eileiterentzündungen bis hin zu Eileiterverklebungen,
- Eileiterschwangerschaften und Unfruchtbarkeit.
Das Beschwerdebild des Mannes kann umfassen:
Entzündungen der Harnröhre, der Hoden oder der Nebenhoden,
Unfruchtbarkeit.
Sowohl beim Mann als auch bei der Frau können weitere Komplikationen sein:
- Rheumatische Entzündungen an Gelenken, an der Wirbelsäule und an den Sehnenansätzen,
- Herzmuskelentzündung,
- Bindehaut- oder Regenbogenhautentzündung des Auges.
All diese Erscheinungen können in Schüben oder chronisch verlaufen.
Wie wird eine Chlamydieninfektion nachgewiesen?
Für den Nachweis muss eine Probe entnommen werden. Zu diesem Zweck kann mit einem Wattetupfer bei der Frau ein Abstrich vom Muttermund und/oder der Harnröhre und beim Mann ein Abstrich aus der Harnröhre entnommen und auf den Erreger untersucht werden. Im Abstrich lässt sich eine Infektion erst 10 bis 14 Tage nach Ansteckung nachweisen. Alternativ kann eine Urinprobe untersucht werden. Bei der Urinprobe ist zu beachten, dass hier Morgenurin verwendet wird oder mindestens 1 bis 2 Stunden die Harnblase nicht entleert wurde. Zudem sollte Erststrahlurin verwendet werden, nicht Mittelstrahlurin. Die Schamlippen dürfen vor der Probengewinnung nicht gereinigt werden. Im Nativpräparat finden sich unreife metaplastische Zellen mit zahlreichen Vakuolen im Zytoplasma und typischen Einschlusskörperchen, allerdings ist die Diagnose so nicht sicher zu stellen. Die empfindlichste Nachweismethode stellt die sogenannte Polymerase-Kettenreaktion (PCR) dar. Kostengünstiger ist ein Enzymimmunoassay (EIA), der zwar auch eine hohe Spezifität von 92-100 % aber eine niedrigere Sensitivität von 65-95 % aufweist, d. h. es gibt auch falsch positive Ergebnisse (der Test ist positiv auf den Erreger, die untersuchte Person aber gesund). Für Frauen bis zum abgeschlossenen 25. Lebensjahr einmal im Kalenderjahr und Schwangere ist eine Untersuchung des Urins mittels PCR eine Leistung aller Krankenversicherungen.
Kann man Chlamydieninfektionen behandeln?
Prinzipiell ist eine Chlamydieninfektion im Frühstadium gut mit Antibiotika zu behandeln, vorausgesetzt man hält die vorgeschriebene Therapiedauer und die Dosierungsempfehlungen genau ein. Therapiestandard außerhalb der Schwangerschaft ist die Gabe von
2x 100 mg Doxycyclin täglich für 7-10 Tage in Tablettenform. Doxycyclin gilt als wirksamste Behandlung der Infektion . Auf jeden Fall sollte der Partner ebenfalls zur gleichen Zeit behandelt werden. Bei verschleppter Infektion hingegen muss viele Wochen behandelt werden; eine Ausheilung ist in diesen Fällen leider auch dann nicht immer möglich. Eine unkomplizierte Infektion des Gebärmutterhalses kann auch mit
1000-1500 mg Azithromycin als Einzeldosis therapiert werden oder bei Koinfektion mit Mycoplasma genitalium mit 500 mg Azithromycin am Tag 1, gefolgt von 250 mg an den Tagen 2 bis 5. Weitere Alternativen sind die Einnahme von
4x 500 mg Erythromycin täglich über 10 Tage oder mit
1x 250 mg Levofloxacin täglich über 10 Tage. Eventuell bestehende Kontraindikationen gilt es natürlich zu beachten. Beim Vorliegen von Mischinfektionen können Kombinationen aus Ofloxacin (2x 400 mg tgl.) plus Metronidazol (2x 500 mg tgl.) über 14 Tage oder aber Amoxicillin/Clavulansäure (2x 875/125 mg tgl., z. B. Amoxi Clavulan AL 875/125 mg®) plus Metronidazol (3x 500 mg tgl.) über 10-14 Tage verordnet werden.
Etwa 4-6 Wochen nach abgeschlossener Therapie kann bei Verdacht auf ein Therapieversagen eine Nachfolgeuntersuchung auf Chlamydien erfolgen. Informieren Sie die Sexualpartner der letzten 60 Tage über ihre Infektion, da eine Mitbehandlung erforderlich ist.
Wie kann man sich vor Chlamydieninfektionen schützen?
Benutzen Sie Kondome, wenn Sie wechselnde Geschlechtspartner haben. Sie schützen vor einer Übertragung, wenn sie konsequent, d. h. auch schon beim Vorspiel, getragen werden. Werden Sexspielzeuge wie Vibratoren von mehreren Personen gemeinsam benutzt, sollten sie vor einer Weitergabe desinfiziert werden. Lassen Sie sich auf Chlamydien untersuchen, wenn Sie den Verdacht haben, sich angesteckt zu haben. Sprechen Sie auch mit Ihrem Partner über Chlamydien und mögliche Krankheitszeichen, um eine Chlamydieninfektion so früh wie möglich erkennen zu können.
Condylomata acuminata (Feigwarzen, Spitze Kondylome):
Diese weltweit häufigste, beim Intimkontakt übertragene Virus-Erkrankung des äußeren Genitale befällt 1-2 % der sexuell Aktiven zwischen dem 15.-49. Lebensjahr. In Deutschland sind pro Jahr etwa 89.000 Neuinfektionen zu erwarten. Bei mehr als 90 % aller
spitzen Kondylome sind humane Papillomaviren (Niedrigrisiko-HPV Typen 6 oder 11) nachzuweisen. Bei bis zu 50 % dieser Veränderungen liegen zusätzliche Co-Infektionen mit den Hochrisiko-HPV-Typen 16, 18 und 45 vor. Diese führen zu einem erhöhten Risiko für die Entstehung von Krebsvorstufen (Dysplasien) von Vulva, Scheide, Gebärmutterhals, Harnröhre sowie der Region um den Anus (Perianalregion). Daher hat etwa jede 4. Frau mit Condylomata acuminata des äußeren Genitale auch schon eine HPV-Infektion des Gebärmutterhalses bzw. der Scheide, bei etwa jeder Zehnten besteht an diesen Stellen bereits eine Dysplasie! Die Condylome treten als blumenkohlartige Tumoren von unterschiedlicher Größe auf. Sie sind weich und in der Regel nicht druckschmerzhaft. Bei
perianalen Warzen ist stets auch eine Enddarmspiegelung angezeigt. Bei Sitz am
Harnröhrenausgang muss eine Harnröhrenspiegelung zum Ausschluss von Kondylomen in der Harnröhre (maximal in 8 % bei vulvärem Befall) folgen. Perianale sowie harnröhrennahe Feigwarzen sind immer zuvor zu entfernen, um endoskopisch keine Verschleppung HPV-infizierter Zellen in den Analkanal sowie die Harnblase zu riskieren.
Subklinische (nicht mit dem Auge sichtbare) Herde lassen sich durch
Essigsäureanfärbung visualisieren. Dabei demaskieren sich sogenannte HPV-getriggerte Epithelhyperplasien nach Betupfen mit fünfprozentiger Essigsäure im Sinne einer klassischen Weißfärbung.
Seit dem Jahr 2007 gibt es eine
Impfung gegen die HPV-Typen 6, 11, 16 und 18. Sie gewährleistet auch eine primäre Prävention gegenüber 90% aller Condylomata acuminata.
Therapeutisch gibt es mehrere Verfahren, welche in einer Leitlinie der
Deutschen STD-Gesellschaft beschrieben sind. Empfehlenswert scheint nach möglicher operativer Abtragung von Kondylomen eine anschließende Behandlung mit
Imiquimod (Aldara® 5 % Creme) für ungefähr 6 Wochen, um verbliebene virusinfizierte Keratinozyten (hornbildende Zellen in der Oberhaut) immunologisch zu eliminieren. Dadurch lässt sich die Rezidivrate von 30-60 % auf 15 % reduzieren. Auch zur Primärbehandlung ist Imiquimod geeignet. Alternativ kann ein aus grünen Teeblättern gewonnenes Catechinpräparat (Veregen® 10 % Salbe) eingesetzt werden. Die Salbe wird für dreimal täglich auf alle äußerlichen Feigwarzen im Bereich der Geschlechtsteile und um den After herum aufgetragen. Die Behandlung mit der Salbe sollte so lange fortgesetzt werden, bis alle Feigwarzen abgeheilt sind, insgesamt jedoch nicht länger als 16 Wochen, selbst wenn während der Behandlung neue Feigwarzen entstehen. Eine weitere medikamentöse Option ist die antimitotische Therapie mit Podophyllotoxin (Wartec®/Condylox®). Die Behandlung erfolgt für maximal 4 Wochen 2-mal täglich für 3 Tage pro Woche. Ebenfalls zur Anwendung kommt Trichloressigsäure (Wartner-Stift®). Es wirkt als Ätzmittel. Diese Behandlung erfolgt über 4 Tage 1- bis 2-mal täglich.
Dellwarzen bilden sich häufig nach einigen Monaten spontan zurück. Sie können aber auch chirurgisch durch Abtragung mit dem scharfen Löffel oder einer speziellen Pinzette entfernt werden. Eine Vereisung ist eine mögliche Alternative.
Man hat sich darauf geeinigt, dass eine Entzündung am Gebärmutterhals vorliegt, wenn bei Betrachtung von Gebärmutterhalssekret bei 400-facher Vergrößerung mehr als 30 Leukozyten pro Gesichtsfeld vorliegen. Im Gram-Präparat finden sich gehäuft intraleukozytäre, gramnegative kaffeebohnenförmige Diplokokken.
Zur kulturellen Anzüchtung werden verschiedene Nährmedien verwandt.
Mittel der Wahl für die Therapie sind 1000 mg
Ceftriaxon (Rocephine® i.v. 1g), intramuskulär oder intravenös, in Verbindung mit 1500 mg
Azithromycin in Tablettenform jeweils als Einmaldosis. Alternativ zu Ceftriaxon kann auch Cefixim, 800 mg, als Einmaldosis in Tablettenform, in Kombination mit Azithromycin eingesetzt werden. Cefixim ist ein Cephalosporin der 3. Generation. 200 mg Doxycyclin tgl. über 7 Tage ist eine Alternative zu Azithromycin.
Granuloma inguinale:
Granuloma inguinale ist eine bakterielle Erkrankung, die charakteristische ulzerierende Läsionen im Genitalbereich aufweist, auch bekannt unter dem Namen Donovanosis nach dem Entdecker der pathognomonischen histologischen Strukturen, oder Granuloma genitoinguinale. 1905 hat der Tropenarzt Charles Donovan die bakterielle Erkrankung zum ersten Mal beschrieben. Der Erreger ist Klebsiella granulomatis (früher Calymmatobacterium granulomatis).
Sie ist
in vielen Entwicklungsländern endemisch. Übertragen wird das Bakterium durch engen Hautkontakt. Sichtbar ist die Geschlechtskrankheit im Bereich der äußeren Geschlechtsorgane sowie im Bereich des Afters. Bis die ersten Symptome auftreten, können wenige Tage oder mehrere Wochen vergehen. Die schmerzlosen Ulzerationen, welche mit Syphilis verwechselt werden können, schreiten letztendlich in die Zerstörung von Gewebe und ausgeprägte Einblutungen fort.
Die Diagnose basiert auf der Anamnese und der klinischen Untersuchung, welche ein schmerzloses Ulkus mit einem charakteristisch gerollten Rand von Granulationsgewebe zeigt. Anders als bei Ulzerationen, die bei Syphilis auftreten, gibt es hier normalerweise keine Lymphknotenbeteiligung. Gewebebiopsien und eine Wright-Giemsa-Färbung helfen bei der Diagnoseerhebung.
Die Therapie kann mit Cotrimoxazol oder Tetracyclinen durchgeführt werden.
- In der ersten Phase der Infektion sind zunächst Bestandteile des Virus (Virus-Antigene) im Blutserum nachweisbar, dazu gehört unter anderem das HBs-Antigen (HBs-Ag). Dieses wird zum Screening auf eine akute Infektion bestimmt. Es handelt sich um ein Eiweiß, das auf der Oberfläche des Virus sitzt.
- Eine Bestimmung von Anti-HBc (Antikörper gegen Hepatitis B-Core-Antigen) würde die Frage nach einer abgelaufenen Hepatitis B klären, ohne Unterscheidung ob ausgeheilt oder chronisch.
- Eine Bestimmung von Anti-HBs (Antikörper gegen Hepatitis B-Surface-Antigen) würde die Frage klären, ob eine Immunität nach Impfung oder Erkrankung besteht.
Herpes genitalis:
Herpes genitalis wird durch Herpes-simplex-Viren der Typen 1 und 2 (HSV-1 und -2) hervorgerufen. HSV-1 wurde ursprünglich fast ausschließlich im Mundbereich nachgewiesen (Lippenherpes), doch mittlerweile muss davon ausgegangen werden, dass aufgrund der zunehmenden Verbreitung oraler Sexualpraktiken bei etwa 30 % der genitalen Herpes-Patientinnen HSV-1 die Ursache ist. Dagegen wird HSV-2 überwiegend durch Geschlechtsverkehr übertragen. Von besonderer Bedeutung ist die Tatsache, dass nicht nur die Läsionen der klinisch manifesten Erkrankung infektiös sind. Auch völlig asymptomatische Virusträgerinnen und -träger können Erreger im Rahmen unbemerkter Reaktivierung der latenten Erkrankung ausscheiden. Herpes genitalis ist eine chronische und potenziell lebenslänglich infektiöse Virusinfektion. Man geht in Deutschland von einer HSV-2-Seropositivität von 14 % bei Erwachsenen aus, bei HSV-1 schätzt man die Seropositivität auf 90 %.
Die Diagnose einer HSV-Infektion wird bei Auftreten der typischen
bläschenförmigen Hauterscheinungen auf gerötetem Grund bereits klinisch gestellt. Häufig findet sich auch ein buntes Bild von Knötchen, Bläschen und Erosionen. Die
Leistenlymphknoten können
geschwollen und
schmerzhaft sein. Handelt es sich um eine Erstinfektion, können zusätzlich ausgeprägte Allgemeinsymptome wie Fieber, Abgeschlagenheit oder Kopfschmerz auftreten. Damit ist ein sogenannter
primärer Herpes genitalis die schwerste und
schmerzhafteste Infektion der Vulva . Rezidive sind meist weniger ausgedehnt nur an einer Stelle der Vulva zu finden. Die Labordiagnostik einer Infektion erfolgt über die Untersuchung von Bläschenflüssigkeit mittels sogenannter Nukleinsäureamplifikationstechnik (NAT), falls zum Zeitpunkt der Untersuchung Bläschen vorliegen. Die für eine schnelle Aussage nach Infektionsbeginn nicht geeigneten serologischen Nachweismethoden sollten frühestens 10 Tage nach Auftreten der ersten Symptome erwogen werden. Die Immunglobulinklassen können getrennt nach IgG und IgM bestimmt werden. Obwohl nicht zur Diagnostik geeignet, kann die differenzierte Bestimmung von HSV-1- und HSV-2-Antikörpern durchaus die Unterscheidung eines genitalen Herpes, der eben vorwiegend HSV-2-assoziiert ist, von anderen Genitalerkrankungen erlauben.
Die Therapie einer Infektion mit Herpes-simplex-Viren richtet sich nach dem allgemeinen Gesundheitszustand und der Schwere der klinischen Manifestation. Bei gutem Gesundheitszustand und nur diskreten Läsionen (Erscheinungsbildern an der Haut) kann die lokale Gabe von
Aciclovir Creme reichen, im Frühstadium sogar
Zinksulfatgel (z. B. Virudermin®) ausreichen.
Systemisch ist ebenfalls Aciclovir Mittel der Wahl, z. B. bei einem primären Herpes genitalis 3x 400 mg oder 5x 200 mg tgl. in Tablettenform über 7-10 Tage, bei Rezidiven 2x 800 mg über 5 Tage. Wenn Aciclovir nicht wirkt, sind Valaciclovir (Valtrex®) und Famciclovir (Famvir®) Alternativen. In den seltenen Fällen einer Aciclovir-Resistenz gilt Foscarnet i.v. als Alternativtherapeutikum. Bei schmerzhaften Läsionen ist zusätzlich ein
Lokalanästhetikum (z. B. Anaesthesulf® Lotio) sinnvoll.
Bei Primärinfektionen sollten die Medikamente mindestens fünf Tage gegeben werden. Im Fall von Rezidiven genügen oft ein bis zwei Tage - vorausgesetzt, die Therapie wird begonnen, sobald sich Beschwerden einstellen.
Zur Rezidivprophylaxe eignet sich gut 500 mg Valaciclovir tgl., über drei Monate gegeben.
HIV:
AIDS ist eine Erkrankung durch ein Virus (HIV), die nicht geheilt werden kann. Das Virus ist über besondere Risikogruppen über die ganze Welt verteilt worden und stellt inzwischen eines der größten Infektionsrisiken bei Sexualkontakten dar.
Das Tückische dieser Infektion ist, dass sie zunächst fast keine Beschwerden verursacht, jedoch im Laufe der Jahre das menschliche Abwehrsystem zerstört, so dass der Mensch dann vielen bis dahin harmlosen Erregern schutzlos ausgeliefert ist. Der Körper altert und verliert Gewicht bis hin zum Tod. Der Erreger befindet sich in Samenflüssigkeit und Blut und wird in erster Linie durch Sexualkontakte und unsaubere, d. h. gemeinsam benutzte, Injektionsnadeln bei Drogenabhängigen übertragen. Sollte das Virus einmal in die Blutbahn gelangen, bleibt es das ganze Leben lang im Körper, und der Mensch würde es an Sexualpartner weitergeben.
Durch Umarmungen, Küssen, Türklinkenanfassen, fremde Toiletten, im Schwimmbad, durch Benutzen einer fremden Kaffeetasse usw. wird das Virus nicht übertragen. Bei Analkontakten kann man sich wesentlich leichter infizieren als bei Scheidenkontakten, da die Darmschleimhaut leichter verletzbar ist. Das Übertragungsrisiko wird durch zusätzliche Genitalinfektionen noch größer. Leider wird das Virus in der Schwangerschaft und bei der Geburt auf einen gewissen Teil der Kinder übertragen. Durch einen Bluttest kann man feststellen, ob eine Infektion vorliegt. Dieser wird in der Schwangerschaft auch von allen deutschen Krankenkassen getragen.
Und wie kann man sich vor AIDS schützen?
Der beste Schutz ist die Vermeidung von Risikokontakten, d. h. Sexualkontakten mit Drogenabhängigen, mit Personen aus Gebieten mit hoher AIDS-Durchseuchung, mit Bisexuellen oder mit Personen, die Geschlechtsverkehr mit verschiedenen Partnern haben. Die Pille schützt zwar vor einer Schwangerschaft, aber nicht vor AIDS! Auch wenn der Geschlechtspartner nicht zu einer Risikogruppe gehört, sollte konsequent ein Kondom benutzt werden.
Ein HIV-Test würde in der Regel 2 Monate nach fraglichem Infektionstermin positiv ausfallen, ein negativer Test schließt somit dann eine HIV-Infektion weitgehend aus. Hat jemand einen festen und treuen Partner, können beide einen HIV-Test machen lassen und nach negativem Ergebnis auf das Kondom verzichten, wenn es nicht zur Verhütung gebraucht wird.
Eine Post-Expositionsprophylaxe ist am erfolgreichsten, wenn sie innerhalb von 2 Stunden begonnen wird. 72 Stunden nach Exposition wird sie nicht mehr empfohlen.
Eine mögliche Indikation ist ein "Kondomunfall" bei vaginalem oder analem Verkehr, wenn der Behandlungsstatus eines HIV-positiven Partners unbekannt ist.
Keine Indikationen sollen sein:
- eine Verletzung an einem alten, weggeworfenen Spritzenbesteck
- ungeschützter Oralverkehr mit einem HIV-positiven Partner (auch bei Aufnahme von Sperma)
- ungeschützter heterosexueller Vaginal- oder Analverkehr mit einem Partner (auch Sexarbeiter), dessen HIV-Status unbekannt ist
Candida intertrigo stellt die häufigste Komplikation einer Intertrigo dar, wobei Adipositas, Diabetes mellitus und allgemeine Abwehrschwäche als begünstigende Faktoren eine Rolle spielen können – ebenso wie Inkontinenz, chronische Bettlägerigkeit, hormonelle Kontrazeption oder Schwangerschaft. Ursache und Folge sind nicht klar voneinander zu trennen, da der Erreger die Entzündung verstärkt und die Entzündung wiederum die Bedingungen für den Erreger begünstigt. Typisch sind relativ scharfe Begrenzungen durch eine dem entzündlich geröteten und nässenden Herdzentrum zugewandte Schuppenkrause. Manchmal treten randwärts kleine Pusteln mit weißgelblichem Inhalt auf. Auch in der näheren Umgebung der juckenden Areale können Papeln und Pusteln als Streuherde auftreten.
Krätze (Scabies):
Bevorzugte Stellen der Krätze, die von Kratzmilben verursacht wird, sind neben der Vulva auch Handgelenke, Ellenbogen, Nabel oder Fußränder. Klinisch finden sich juckende Knoten sowie typische Hautveränderungen mit Exanthemen, Milbengängen und sekundären Kratzeffekten. Diagnostiziert wird klinisch, wobei der Nachweis der Kotballen entscheidend ist. Eingesetzt werden bei der Patientin und deren engen Kontaktpersonen lokal wirksame Präparate mit Benzylbenzoat, z. B. Antiscabiosum® Emulsion (1. Wahl in Schwangerschaft und Stillzeit) oder Crotamiton, z. B. Crotamitex® Salbe oder Permethrin, z. B. Infectopedicul®. Gerne wird systemisch kombiniert mit Ivermectin. Auch wichtig sind Umgebungsmaßnahmen. Kleider, Bettwäsche, Handtücher oder andere Gegenstände mit längerem Körperkontakt (Blutdruckmanschette, Pantoffeln, Stofftiere etc.) sollten bei mindestens 50 °C für wenigstens 10 Minuten gewaschen oder mit Hilfe eines Heißdampfgeräts dekontaminiert werden. Es wird auch empfohlen, Wäsche in verschlossenen Plastiksäcken drei Tage lang zu lagern.
Lichen planus (Lichen ruber planus):
Der Lichen planus ist eine Hauterkrankung mit roten Knötchen an der Haut. Besonders häufig sind die Innenseite der Handgelenke und die Vorderseite der Schienbeine betroffen. Veränderungen finden sich auch an der Wangenschleimhaut und den Genitalien. Die anogenitale Haut erscheint unruhig mit gekörnter bis hin zu kopfsteinpflasterartiger Oberflächenstruktur. Am Introitus vaginae findet man ein glänzendes Erythem.
Pathognomisch für die Frühform sind weißliche Strukturen, die teilweise netz- oder gitterförmig ausgebildet sind (Wickham-Striae). Am Genitale sind davon die großen und kleinen Labien sowie der Sulcus interlabialis betroffen. Auch an der Wangenschleimhaut können sich scharf begrenzte Rötungen mit weißlichem Randsaum entwickeln. Ein Lichen planus in seiner Frühform führt zu Juckreiz. Die schmerzhafteste Dermatose mit brennenden Beschwerden ist dann das
Spätstadium eines Lichen planus, der
Lichen planus erosivus. Typischerweise finden sich scharf demarkierte erosive Erytheme neben der Vulva auch in der Vagina und der Mundschleimhaut. Die Diagnose wird histologisch gestellt. Therapeutisch wird eine lokale Kortikosteroidtherapie bevorzugt. Vor allem bei Ausdehnung auf die Vagina kommt im Off-Label-Use die Anwendung von Hydrocortison-Rektalschaum in Frage. Ein Lichen planus der Vulva/des Vestibulums und auch der Mundschleimhaut ist mit einem um 5 % bezifferten Karzinomrisiko verbunden. Aufgrund eines möglichen schnellen Progresses sollte die Kontrolle eines vulvovaginalen Lichen planus alle 6 Monate erfolgen.
Lichen sclerosus:
Der Lichen sclerosus, auch Weißfleckenkrankheit genannt, ist die häufigste Dermatose des Genitale, bis zu einem Prozent der Frauen sind betroffen. Er tritt bei Mädchen und Frauen jeden Alters auf, mit zunehmenden Alter allerdings etwas häufiger. Die Ursache dieser Erkrankung ist letztlich unklar. Typisch ist das
porzellanweiße Epithel (weißliche Hautbezirke) mit glatter Oberfläche, teils zusammen mit umschriebenen Hyperkeratosen (übermäßiger Verhornung der Haut). Ein früher Lichen sclerosus ist als glänzende Hautrötung oder fleckförmige Depigmentierung an der Klitoris oder den kleinen Schamlippen sowie in den Furchen zwischen den großen und kleinen Schamlippen (interlabiale Sulci) sichtbar. Die Veränderungen können symptomlos bleiben oder gehen mit Juckreiz, seltener mit brennenden Beschwerden einher.
Schrumpfungsprozesse an den kleinen Schamlippen sind typisch, es kann zu einer Verengung der Scheide kommen. Mit einer Stanzbiopsie kann die Diagnose gesichert werden. Die Biopsie sollte in zwei Arealen mit einer Stanze von mindestens 4 mm Durchmesser erfolgen. Therapie der Wahl ist die lokale Anwendung von
hochpotenten Glukokortikoiden (z. B. Clobetasol- oder Mometasonfuroat in Salbenform) über einen Zeitraum bis zu 3 Monaten in absteigender Dosierung, beispielsweise vier Wochen lang einmal täglich, dann vier Wochen lang nur noch an jedem zweiten Tag und im dritten Monat noch zweimal pro Woche. Eine
rückfettende Salbe, z. B. Deumavan®, oder eine Hautpflege mit Mandelöl ist danach angezeigt, um den Feuchtigkeitsverlust zu reduzieren und die mechanische Belastung der Haut zu reduzieren. Das Genitale sollte nur mit klarem Wasser gewaschen werden. Der Lichen sclerosus neigt zu Rezidiven und kann über viele Jahre immer wieder aufflammen und sich dann auch als therapieresistent erweisen. Bei 20-30 % der Frauen mit Lichen sclerosus werden Autoimmunerkrankungen beschrieben. Der Lichen sclerosus stellt keine Krebsvorstufe dar, sondern eine gutartige chronische Hauterkrankung mit überwiegendem Genitalbefall. Jedoch liegt das Risiko für die Entwicklung eines Plattenepithelkarzinoms bei 1-4 % aller Fälle. Daher sollten Patientinnen mit Lichen sclerosus 1-2x jährlich kontrolliert werden.
Links:
Fachbereich Dermatologie des Katholischen Klinikums Bochum - Ausführungen zum Lichen sclerosus
Lichen sclerosus Deutschland e.V. - Bundesweite Selbsthilfe für betroffene Menschen
Lichen simplex chronicus (Sonderform des atopischen Ekzems):
Während bei der akuten Form eines Ekzems Erytheme, Nässen, Bläschen, Papeln und Krusten auftreten, finden sich bei der chronischen trockenen Form
Hautverdickungen, Lichenifizierung (grobe Hautfalten) und Schuppung . Die Haut weist eine
blasse matte Rötung auf. Diese Hauterkrankung kann durch eine chronisch umschriebene Traumatisierung der Haut oder als Folge eines atopischen Ekzems entstehen.
Juckreiz und Brennen mit dem Bedürfnis zu kratzen bestimmen die Symptomatik. Typisch ist, dass die Nachtruhe stark gestört wird. Die Diagnose wird häufig durch eine Biopsie gestellt. Therapie der Wahl ist die lokale Anwendung von hochpotenten Glukokortikoiden über einen Zeitraum von mindestens einen Monat, gelegentlich bis zu 3 Monaten.
Lues, Syphilis (Treponema pallidum):
Die durch Bakterien hervorgerufene Syphilis, auch Lues genannt, ist bei uns seltener geworden, in anderen Ländern der Erde ist sie noch wesentlich häufiger. Die Übertragung erfolgt ausschließlich durch direkten Kontakt mit Haut oder hautnahen Schleimhäuten infizierter Personen, das heißt bei Sexualkontakten. Typisch für den Beginn einer Syphilis ist ein schmerzloses Geschwür, scharf begrenzt, flach, mit einem gelblich belegten Grund und derben Randwall im Geschlechtsbereich (Ulcus durum), das nur sehr langsam über ca. 4 Wochen abheilt (
Primärstadium , Lues I). Meist findet es sich an der vorderen oder hinteren Kommissur (Vereinigungsstellen der beiden großen Schamlippen), an einer kleinen Schamlippe oder am Gebärmutterhals. Ansonsten bestehen zunächst keine Beschwerden oder Veränderungen.
Acht Wochen nach der Ansteckung kommt es oft zu grippeartigen Beschwerden wie Fieber, Abgeschlagenheit oder Kopf- und Gliederschmerzen. Die Lymphknoten am ganzen Körper sind geschwollen. Die Erkrankung ist nun in ein
generalisiertes Stadium übergegangen. Nach zehn Wochen erscheint bei den meisten Erkrankten ein Hautausschlag (Exanthem). Zunächst sind es nur schwachrosa gefärbte Flecken, die sich in kupferfarbene Knötchen (Papeln) verwandeln. Breite Papeln, die besonders in Hautfalten auftreten, nennt man Condylomata lata. Wenn diese aufgehen und nässen, ist die austretende Flüssigkeit hoch infektiös. Seltener treten auch Schleimhautveränderungen im Mund und an den Genitalien auf. Manchen Patientinnen fallen die Haare aus. Alle Hauterscheinungen (Syphilide) heilen nach ungefähr vier Monaten ab. Unbehandelt kommen sie innerhalb verschiedener Zeitabstände wieder. Typischerweise tritt bei allen Hauterscheinungen der Syphilis wenig bis kein Juckreiz auf.
Die Syphilis ist eine der gefährlichsten Geschlechtskrankheiten, da sie ohne Behandlung den Körper und schließlich das Gehirn im Verlauf der Jahre schwerst schädigt. Der mikrobiologische Nachweis erfolgt primär serologisch über den Antikörpernachweis im Rahmen einer Stufendiagnostik. Jede Schwangere wird auf Syphilis untersucht, da der Erreger schon im Mutterleib auf das Ungeborene übertragen wird.
Die Frühsyphilis wird einmalig mit 2,4 Mio. IE
Benzathin-Benzylpenicillin (z. B. Pendysin® 1,2 Mio I.E.) intramuskulär behandelt, die Spätsyphilis dreimalig im wöchentlichen Abstand.
Lymphogranuloma venereum:
Das Lymphogranuloma venereum ist eine durch das obligat intrazelluläre gramnegative Bakterium Chlamydia trachomatis der Serovare L1–L3 hervorgerufene Geschlechtskrankheit. Die Infektion führt zu einem ganz charakteristischen, regionalen, genitoanalen Symptomenkomplex. Das LGV ist in Indien, Afrika und Lateinamerika sowie im Südosten der USA endemisch, in Europa kommt es selten vor. Chlamydieninfektionen mit den Serovaren L1–L3 rufen einen ganz charakteristischen regionalen genitoanalen Symptomenkomplex hervor. Etwa zwei Wochen nach Inokulation tritt an der Eintrittsstelle (Penis, vordere Urethra, Vulva, Vagina, Zervix, Anus) eine kleine Erosion oder Ulzeration auf, die oft unbemerkt abheilt (Primärstadium). Nach weiteren zwei Wochen treten Systemzeichen und schmerzhafte inguinale Lymphknotenschwellungen auf. Diese bis zu faustgroßen Bubonen schmelzen eitrig ein, rupturieren oder bilden Fisteln. Bei Analverkehr sind primär Diarrhö und Proktitis möglich (Sekundärstadium). Bei Frauen kann die Infektion zu Zervizitis und Salpingitis führen.
Mycoplasma genitalium:
Mycoplasma genitalium ist neben Chlamydia trachomatis und Neisseria gonorrhoe ein Erreger, der
Entzündungen am Gebärmutterhals hervorrufen kann. Der Erreger ist anders als Mycoplasma hominis und Ureaplasma urealyticum schwierig anzüchtbar, da er sehr anspruchsvoll ist und extrem langsam wächst. Ein Nachweis mittels Nukleinsäure amplifizierender Technik (NAAT) ist möglich, ebenso eine Resistenztestung. Die Behandlung erfolgt durch 2x 100 mg Doxycyclin pro Tag über 7 Tage, gefolgt von 500 mg
Azithromycin am Tag 1, gefolgt von 250 mg Azithromycin für weitere 4 Tage in Form von Tabletten, alternativ aufgrund einer starken Zunahme von Resistenzen gegen Azithromycin Tabletten mit 400 mg
Moxifloxacin (Avalox® 400 mg Filmtabletten) tgl. über 7-14 Tage. Aufgrund der vielfältigen und teilweise schwerwiegenden Nebenwirkungen von Moxifloxacin ist eine strenge Indikationsstellung geboten.
Schamlaus (Pediculosis pubis):
Die Schamlaus und deren Nissen sitzen an den Haaren, dabei sind die Prädilektionsstellen der behaarte Genital- und Perinealbereich, seltener werden auch die Achselhaare, die Augenbrauen und die Wimpern befallen. Neben den oft schon blickdiagnostisch erkennbaren Läusen sind die „Taches bleues“ auffällig: Blaue juckende Flecken, den Saugstichspuren der Läuse entsprechend. Die betroffene genitoanale oder axilläre Region sollte vollständig rasiert werden. Alternativ ist eine Off-Label-Therapie mit Dimeticon topisch möglich. Dimeticon wirkt physikalisch, indem es in Tracheen der Nissen und Läuse eindringt und bei diesen nach wenigen Minuten zum Ersticken führt. Eine offizielle Zulassung besteht allerdings nur für die Behandlung der Kopfläuse (Pediculus capitis).
Streptokokken der Gruppe A können unter anderen auch eine eitrige Angina tonsillaris bzw. Pharyngitis, ein Erysipel und Scharlach hervorrufen.
Trichomonaden:
Trichomonaden werden häufiger bei Sexualkontakten übertragen. Die Infektion kann selten aber auch in Form einer Schmierinfektion über Gegenstände oder gemeinsam benutzte Toiletten erfolgen. Die Erreger führen zu einem
lästigen dünnflüssigen grüngelben Ausfluss meist zusammen mit einem
brennenden Schmerz . Die Beschwerden können zeitweise auch geringer ausgeprägt sein oder zeitweise sogar ganz fehlen. Die Infektion ist auf die Scheide beschränkt, die Gebärmutter wird nicht befallen.
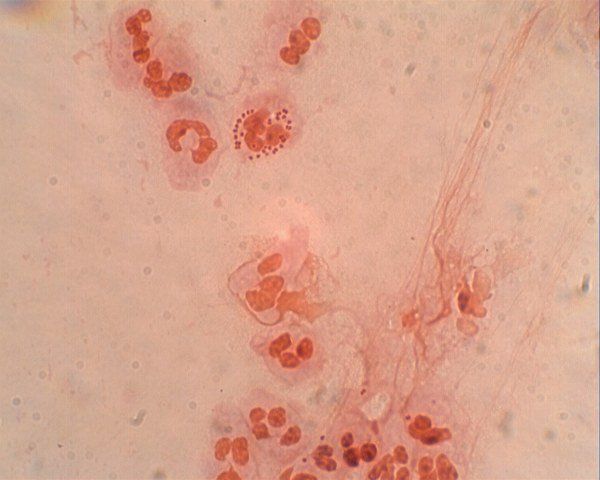
Bei der Spiegeleinstellung zeigt sich der gelbe Ausfluss mit einer charakteristischen Bläschenbildung. Der Erregernachweis gelingt mittels Phasenkontrastmikroskopie im Nativpräparat (mehr als 100 Leukozyten im Gesichtsfeld), Kultur oder Nukleinsäureamplifikationstechnik. Trichomonaden sind zuckende, begeißelte Einzeller mit einer undulierenden Membran ähnlich dem Flossensaum einer Flunder auf einer Zellseite und haben etwa die Größe eines Leukozyten. Während bei der frühen Infektion aufgrund einer hohen Erregerdichte meist schon der mikroskopische Nachweis der Trichomonaden gelingt, ist die Mikroskopie bei der chronischen Infektion oft falsch negativ, da nur wenige Trichomonaden vorhanden sind. Auffällig ist in diesem Stadium jedoch immer noch die hohe Leukozytenzahl im Ausfluss.
Trichomonaden haben einen anaeroben Energiestoffwechsel und sind deshalb gegen
Metronidazol empfindlich. Da die Harnröhre häufig mitbeteiligt ist, sollte
systemisch behandelt werden, z. B. mit 1x 2000 mg als Einmaldosis oder 500 mg zweimal täglich über 7 Tage. Eine Eintagestherapie ist bei Frauen nicht immer ausreichend. Wichtig ist eine Mitbehandlung aller Partner der letzten 60 Tage. Die Wiederherstellung einer gesunden Vaginalflora kann durch die lokale Applikation von Laktobazillen unterstützt werden.
Differentialdiagnostisch ist das Ulcus molle vom Ulcus durum als Primäraffekt der Syphilis zu unterscheiden.
Nach den Europäischen Leitlinien (IUSTI) von 2010 besteht die First-Line-Therapie aus 250 mg Ceftriaxon i.m. als Single-Shot, alternativ einmalig 1000-1500 mg Azithromycin oral.
Vaginalkandidose:
Im Laufe ihres Lebens erleiden drei von vier Frauen mindestens einmal eine Pilzinfektion (Mykose) der Scheide, auch Vaginalkandidose genannt, die meisten erkranken sogar häufiger - durchschnittlich bis zu vier Mal. Nach Schätzungen gibt es in Deutschland zwischen drei und fünf Millionen Erkrankte sowie eine Millionen Ersterkrankungen jährlich. Diese erfolgen meistens im Alter zwischen 18 und 30 Jahren. Grundlage jeder Infektion ist nämlich das Vorhandensein von Rezeptoren auf der Vaginalhaut, an die sich der Erreger festsetzen kann. Die Rezeptoren sind estrogenabhängig, weshalb manifeste Infektionen frühestens mit der Geschlechtsreife eintreten und in der Postmenopause wieder verschwinden. Die Anzahl der Rezeptoren kann schwanken, womit es zu unterschiedlichen Intensitätsphasen der Infektion kommen kann. Bei Frauen besteht prämenstruell wegen der progesteronbedingten Zytolyse ein hohes Angebot an Glykogen, das durch Lactobazillen zu Säure und kurzkettigen Zuckern abgebaut wird. Ein Paradies für Pilze, was den typischen Ausbruch der Vaginalkandidose in der 2. Zyklushälfte erklärt. Pilze und Lactobazillen sind häufig vergesellschaftet, Ausnahmen sind Antibiotikatherapien, nach denen die Keime vorübergehend fehlen können. Aus diesem Grund haben Mykose-Patientinnen fast nie eine Harnblasenentzündung. Die Bakterien einer gesunden Vaginalbesiedlung schließen das aus, anderseits fördern sie den Pilz. Verursacher einer Scheidenpilzinfektion ist ein Hefepilz der Gattung Candida. Er findet sich in geringen Mengen zum Beispiel auch im Darm oder auf der Vaginalhaut gesunder Menschen. Erst bei Veränderungen des Scheidenmilieus, etwa durch Stress (erhöhter Cortisolspiegel) oder hormonelle Schwankungen, kann es zur starken Vermehrung des Pilzerregers und damit zur Infektion kommen. Zudem kann der Hefepilz auch von außen in den Körper gelangen. Ansteckungsmöglichkeiten finden sich überall dort, wo es warm und feucht ist, zum Beispiel im Schwimmbad, in einer nicht gepflegten Sauna, durch Handtücher und auch beim Geschlechtsverkehr. Zu den Symptomen der Vaginalmykose zählen
starker Juckreiz und Brennen im Genitalbereich sowie
gelb-weißer, oft flockiger Ausfluss . Häufig bildet sich ein Ekzem in der Scheidenumgebung bis zum Anus.
In über 90 % der Fälle ist Candida albicans der Erreger. Morphologisch imponieren rötliche und weißliche Plaques sowie Erosionen. Im Nativpräparat sieht man dann Pseudohyphen und vermehrt Granulozyten. Finden sich viele Sprosszellen (Blastosporen), die nur halb so groß erscheinen wie bei Candida albicans, so könnte eine Besiedlung durch
Candida glabrata vorliegen. Dieser Hefepilz wird bei etwa
2 % der Fälle gefunden. Er erzeugt eine mildere klinische Beschwerdesymptomatik.
Die Infekte mit Candida albicans sind in der Regel lokal leicht behandelbar. Die Phase der sogenannten Myzelbildung ist zugleich auch die Schwachstelle des Erregers, da er in diesem Moment viele Angriffspunkte für eine medikamentöse Behandlung mit Antimykotika wie Clotrimazol, Fluconazol oder Itraconazol bietet. Das bekannteste Medikament
Clotrimazol erfasst alle Pilzerreger, die Pseudomyzel bilden wie beispielsweise Candida albicans. Daneben gibt es zum Beispiel auch ein Präparat mit Fenticonazol (Fenizolam®). Clotrimazol wirkt auch (schwächer) auf bakterielle Keime wie Gardnerella vaginalis und antientzündlich. Grundstein ist eine gründliche Lokalbehandlung. Diese muss vaginal sowie in der unmittelbaren Umgebung der Scheide, um die Klitoris, unter der Klitoris-Vorhaut der Patientin und bis zum Po erfolgen, da auch dort Pilze siedeln, die unbehandelt zu einem erneuten Rezidiv führen können. Ratsam ist eine Rasur der Intimbehaarung vor der Therapie, da die Keime auch dort siedeln können. Körperfern überlebt Candida albicans nur wenige Minuten, sodass weder die Textilien noch Haushaltsgegenstände wie Toiletten desinfiziert werden müssen. Das Wirkoptimum von Clotrimazol liegt im sauren Bereich, da ein niedriger vaginaler pH-Wert die Pilze gegen den Wirkstoff empfindlicher macht. Einigen Clotrimazol-Präparaten ist deshalb
Milchsäure zugesetzt. Der Juckreiz verschwindet meist erst am 3. Behandlungstag. Nach Behandlung einer Mykose ist es nicht mehr sinnvoll Milchsäure einzusetzen, da die Säure auf der noch gereizten und empfindlichen Haut brennt. Diese Haut braucht nur noch Pflege und Regeneration mit fetthaltigen Cremes wie
Deumavan® (Vulva), Gelen wie
Gynomunal®, die regenerierendes Vitamin E und Hopfen enthalten oder Befeuchtungsovula wie
Kadefungin® Befeuchtungsovula mit Hyaluronsäure, Vitamin A und E. Bei ausgeprägter Symptomatik ist 150 mg Fluconazol, zweimal eingenommen im Abstand von 2 Tagen, eine Alternative.
Während Candida albicans,
Candida parapsilosis und
Candida tropicalis hochsensibel auf die Behandlung mit Azolen reagieren, werden Pilzarten wie
Candida glabrata und Candida krusei, die keine bzw. kaum Myzelien bilden,
mit Ciclopiroxolamin (z. B. INIMUR myko®) und Nystatin als Mittel der Wahl behandelt. Dazu werden zwei Tuben Ciclopiroxolamin Creme á 35 g verwandt. Die Creme wird zweimal täglich tief vaginal eingeführt, auch die Schamlippen, die Vorhaut der Klitoris, der Scheideneingang der Hinterdamm und die Analfalten werden eingecremt. Nystatin in Scheidentablettenform sollte jeweils morgens und abends tief intravaginal eingeführt werden. Die Behandlung sollte über 15 Tage erfolgen. Begleitend sollte vor Therapiebeginn die Intimbehaarung rasiert werden. Um Rezidive zu vermeiden, ist es wichtig, vor der eigentlichen Therapie Keim-Reservoire wie Zahnprothesen bei Partnern zu untersuchen und zu behandeln. Candida glabrata ist ein
typischer Prothesenkeim, der einer professionellen Zahn- und Prothesenreinigung zugänglich ist. Dazu gibt es Lutschtabletten mit Nystatin und Amphotericin B.
Problematisch sind die immer wiederkehrenden Entzündungen. Von einer chronisch rezidivierenden Pilzinfektion des Genitale spricht man, wenn sie
mindestens viermal im Jahr auftritt. Häufig besteht dann eine genetische Veranlagung (Genpolymorphismen des Mannose-bindenden Lektins), eine schwache Glukosetoleranz, ein Diabetes mellitus oder eine generelle Neigung zu Atopien oder Allergien. Solche chronisch rezidivierenden Fälle mit starkem Befall der Vulva bedürfen in der Regel der Therapie in Tablettenform, denn es ist damit zu rechnen, dass die Pilze schon in tiefere Hautschichten vorgedrungen sind und dort therapieresistente Sporen gebildet haben. So können die Pilze auch auf Spiralen,
Verhütungsringen, Vaginalpiercings sowie im Mund auf Zahnstein und Belägen siedeln, welche im Zuge der Therapie entfernt werden müssen. Auf eine gleichzeitige topische Behandlung sollte nicht verzichtet werden, da man mit Tabletten die Vulva und die Umgebung der Klitoris nicht erreichen kann. Zudem ist die Partnertherapie erwägenswert, bei asymptomatischen Sexualpartnern wird sie allerdings nicht empfohlen. Die Bestimmung der Candida-Art ist notwendig, weil es selten Arten gibt, die gegen Fluconazol und andere Triazole nicht empfindlich sind (z. B. Candida krusei).
Zur Behandlung wurde lange eine sogenannte
degressive Therapie mit dem Wirkstoff Fluconazol (z. B. Flucobeta® 200 mg Hartkapseln) empfohlen (nach Donders et al. 2008):
- Erste Woche Initialtherapie: je 200 mg Tag 1, Tag 3, Tag 5
- 14 Tage später Pilzkultur, wenn negativ: 1x 200 mg wöchentlich 2 Monate lang
- 14 Tage später Pilzkultur, wenn negativ: 1x 200 mg zweiwöchentlich 4 Monate lang
- 14 Tage später Pilzkultur, wenn negativ: 1x 200 mg monatlich 6 Monate lang
Bemerkung: Falls Pilzkultur positiv, Rückgang auf den vorigen Therapielevel
Aktuell wird eine Langzeittherapie mit 200 mg Fluconazol empfohlen, anfangs drei Tage täglich, danach eine Dosis pro Woche über mindestens 6 Monate. Alle 4 Wochen sollte auch eine lokale Therapie erfolgen.
Itraconazol kann alternativ eingesetzt werden, vor allem, wenn auch andere Mykosen wie eine Onychomykose (Nagelpilz) oder Pityriasis versicolor vorliegen. Drei Tage täglich 200 mg Itraconazol gefolgt von einer Dosis von 200 mg pro Woche über mindestens 6 Monate sollen eingenommen werden. Zu einer Behandlung von Nagelpilz gehört allerdings auch das Abtragen der vom Pilz geschädigten Nagelmasse sowie die nachfolgende tägliche Therapie mit einem sporoziden und wasserlöslichen Nagellack.
Auch im Falle einer systemischen Therapie darf nicht auf eine
topische Behandlung verzichtet werden, da innere Medikamente den äußeren Vaginalbereich, wie die Umgebung der Klitoris, nicht erreichen. Diese Lücke wird durch die topischen Präparate geschlossen, die alle 4 Wochen eintägig angewandt werden sollten. Damit wird der Erreger von zwei Seiten aus behandelt und konsequent beseitigt.
In Einzelfällen kann eine Suche nach
Infektionsquellen im Körper hilfreich sein. Abstriche vom
Mund beider Partner (von der Zunge und unterhalb der vorderen Zahnhälse), bis zu drei
Stuhl proben der Patientin von verschiedenen Tagen (Pilze im Darm sind nicht gleichmäßig verteilt), eine
Sperma probe bei Verdacht auf Candida glabrata oder ein Abstrich von der
Glans penis bei Diabetikern kommen in Frage. Die Sanierung der Mundhöhle kann über eine gründliche professionelle Zahnreinigung, eine Desinfektion von Zahnersatz oder Zahnspangen mit Ultraschall und Reinigungstabletten, Lutschtabletten mit Amphotericin B (viermal täglich über 5 Tage), eine Darmsanierung mit Amphotericin B (z. B. Biofanal® 100 Dragees, 2x2 tgl. über 25 Tage) erfolgen. Auch die Zufuhr von Bierhefe-Produkten aus der Apotheke (Backhefe, Bäckerhefe, Saccharomyces cerevisiae) führt zu einer natürlichen Verdrängung von Darmpilzen. Systemische Antimykotika wirken im Darm nicht, da sie vollständig resorbiert werden. Sinvoll ist es, eine Darmsanierung erst nach einer Mundbehandlung zu beginnen, weil dadurch der Nachschub der Pilze aus dem Mund entfällt.
Dermatosen können ebenfalls Juckreiz auslösen. Wenn keine Pilze nachweisbar sind oder das Anitmykotikum (Mittel gegen Pilzinfekte) nicht geholfen hat, sollte an eine Dermatose wie das atopische Ekzem, Lichen sclerosus, Lichen planus oder Psoriasis inversa gedacht werden.
| Produkt | Antimykotikum | Kortikosteroid | Antiseptikum |
|---|---|---|---|
| Nystalocal® | Nystatin | Dexamethason | Chlorhexidin |
| Lotricomb® | Clotrimazol | Betamethason | - |
| Decoderm tri® | Miconazol | Fluprednidin | - |
| Vobaderm® | Miconazol | Fluprednidin | - |
Wie die Feigwarzen wird die Verruca vulgaris durch eine Infektion der Epithelzellen mit dem Human Papilloma Virus (HPV) ausgelöst. Zu den häufigsten Erregern zählen HPV-2 und HPV-4. Weitere mögliche Auslöser sind HPV-1, 3, 26, 29 und 57. Die Infektion führt zu einer Proliferation der Epithelzellen, welche die makroskopisch sichtbaren Hautveränderungen erzeugt.
Es finden sich einzeln oder in Gruppen, meistens scharf begrenzte, flach halbkugelige oder spitze Auswüchse der Haut; selten auch ganz flach, überwiegend an Händen und Füßen.
Vulvodynie/Vestibulodynie:
Bei Verdacht auf eine Vulvodynie bzw. Vestibulodynie können Fragen weiterhelfen
- zur allgemeinen und gynäkologischen Vorgeschichte,
- zur sexuellen Zufriedenheit,
- zur Partnerschaft und
- nach Psychotherapien sowie zur Einnahme von Psychopharmaka.
Anschließend erfolgt die Diagnose klinisch. Gynäkologische Infektionen sollen mittels Nativpräparat ausgeschlossen bzw. behandelt werden (möglichst nicht lokal). Des Weiteren kann eine pH-Messung sowie ggf. eine Pilzkultur Aufschluss bringen. Bakteriologische Abstriche und histologische Untersuchungen sind dagegen nicht notwendig. Eine lokalisierte Schmerzzone kann mit dem sog. Q-Tip-Test exploriert werden.
Patientinnen mit Vulvodynie bzw. Vestibulodynie leiden signifikant häufiger als gesunde Frauen an Komorbiditäten, wie
- chronischen Blasenschmerzen,
- Reizblase (overactive bladder)
- Reizdarm,
- kraniomandibulärer Dysfunktion,
- Fibromyalgie,
- Migräne,
- Endometriose.
Die Pathophysiologie ist noch nicht vollständig geklärt. Eine Hypothese stellt die immunvermittelte veränderte Schmerzwahrnehmung in der Vulva nach wiederholter lokaler Reizung dar. Dieser Schmerz tritt meist in Verbindung mit psychosozialem Stress oder emotionalen Konflikten auf. So leiden viele Patientinnen mit Vulvodynie u. a. an Angststörungen, Depression, Enttäuschung, Kränkung, Panikattacken oder Schlafmangel bei oft perfektionistischer Persönlichkeit.
Als Basisbehandlung gilt folgendes:
- Beenden Sie alle unnötigen oder nicht eindeutig indizierten Lokaltherapien mit Antimykotika, Antiseptika oder Antibiotika! Häufig wurden Antimykotika bereits ausgiebig eingesetzt.
- Stellen Sie die Intimhygiene auf den Prüfstand: Vulva und Vestibulum sollten nur mit Wasser gewaschen und sanft abgetupft werden. Eine Pflege kann ggf. mit einer milden, nicht zu fetten und parfumfreien Creme erfolgen. Die Intimregion sollte nicht mit dem Fön getrocknet werden!
Es existiert folgende Einteilung:
1.
Generalisiert
- provoziert (sexueller Kontakt, nicht sexuell oder beides)
- unprovoziert
- gemischt (provoziert und unprovoziert)
Bei einer generalisierten Vulvodynie, wie bei allen chronischen Schmerzsyndromen, gibt es eine große Liste empfohlener Therapien. Insbesondere Physiotherapie des Beckenbodens (Unterschied zwischen Anspannung und Entspannung, Dehnungsübungen) , Akupunktur, Yoga, Autogenes Training und eventuell Meditation haben sich wohl bewährt. Empfehlenswert ist die Kombination mit oral wirksamen trizyklischen Antidepressiva (Amitriptylin) und Antikonvulsiva. Lokale Therapien bringen meist keinen Behandlungserfolg.
2.
Lokalisiert (einschließlich Vestibulodynie, Klitorodynie, Hemivulvodynie)
- provoziert (sexueller Kontakt, nicht sexuell oder beides)
- unprovoziert
- gemischt (provoziert und unprovoziert)
Epidemiologische Untersuchungen haben gezeigt, dass
lokalisierte, provozierte, Vestibulodynien über 2/3 der Fälle mit schmerzhafter Vulva ausmachen.
Manchmal klagen die Patientinnen um den
Ausgang der Bartholin-Drüsen und die neben der Harnröhre gelegenen
Skeneschen Drüsengänge über
punktförmige Schmerzen oder Brennen. Die Schmerzen sind auslösbar bei Berührung, zum Beispiel
beim Einführen eines Tampons oder Penetration des Partners. Eine mögliche Ursache ist eine chronisch-entzündliche Erkrankung, die im Scheidenvorhof auftritt, am häufigsten eine chronische Candida-Infektion des unteren Genitaltrakts. Allerdings bleibt bei einigen Patientinnen der Pilznachweis aus.
Manchmal findet sich ein Erythem um die Mündungsstelle der Ausführungsgänge der Bartholin-Drüsen (Glandulae vestibulares majores) und ein auslösbarer Schmerz auf Berührung. Es handelt sich in diesem Fall nicht um eine Entzündung, sondern um eine
Ausstülpung der Haut des Bartholindrüsenausgangs. Durch eine erzwungene Reepithelialisierung nach mehrfacher milder Denaturierung (Albothyl, Off-Label-Use) soll sie meist ausheilen.
Auch
anatomische Anomalien können vorliegen. Am Häufigsten soll ein ausgeprägtes, sogenanntes quer gelegenes Frenulum vestibuli am hinteren Introitus sein. Die zweithäufigste Anomalielie betrifft das Hymen, ein insbesondere dorsal erhöhtes Hymen (Hymen altus basale). Die Außenfläche dieses Hymenteiles ist in den meisten Fällen sehr stark gerötet und druckdolent. Medikamentöse Behandlungen sollen bei anatomischen Anomalien und chronifiziertem, also länger als 1 Jahr bestehendem Krankheitsbild nicht mehr zielführend sein.
Bemerkung: Die Beschreibung dieses Krankheitsbildes soll bitte nicht den Eindruck erwecken, dass ich eine besondere Expertise in der Diagnostik oder Therapie besitze.
Zyklische Vulvovaginitis:
Unter einer zyklischen Vulvovaginitis versteht man ein
vom Östrogenspiegel abhängiges Beschwerdebild . Es ist
während der Gelbkörperphase am stärksten ausgeprägt. Schmerzen am Genitale, welche auch in Beziehung zum Koitus stehen, prägen das Erscheinungsbild.
Die Symptome werden direkt postkoital verstärkt bemerkt und treten am folgenden Tag am stärksten auf . Postuliert wird eine Überempfindlichkeitsreaktion gegenüber Candida-Antigen. Durch die bestehende Immunreaktion kann Candida während der symptomatischen Phase nicht immer nachgewiesen werden. Kulturen sollen während der asymptomatischen Phase entnommen werden. Eine
längere Erhaltungstherapie mit Antimykotika bringt Erleichterung und sollte bis zu 6 Monate erfolgen.
Zytolytische Vaginose:
Die Zytolytische Vaginose ist durch eine erhöhte Anzahl von Laktobazillen unterschiedlicher Größe sowie durch eine Zytolyse der Zellen des Vaginalepithels gekennzeichnet, was durch das Vorhandensein von nackten Kernen und zytoplasmatischen Trümmern erkennbar ist. Typischerweise fehlen andere Bakterien. Das Erscheinungsbild ähnelt stark dem einer Vaginalkandidose. Die Betroffenen klagen über ein Brennen an der Vulva (häufiger als über Juckreiz). Der Erfahrung nach sind die Symptome beim Aufwachen meist nicht vorhanden oder mild und entwickeln sich erst nach dem Aufstehen. Bei Frauen, die keine hormonellen Verhütungsmittel anwenden, beginnen die Symptome meist mit dem Eisprung und verschlimmern sich bis zum Einsetzen der Menstruation. Während der Menstruation lassen die Symptome tendenziell nach. Einige Frauen beschreiben auch terminale/postmiktionelle Dysurie und Trockenheit/Dyspareunie.
Die Untersuchung der Vulva ist normalerweise unauffällig, manchmal kann jedoch ein diskretes Erythem vorhanden sein. Der typische Vaginalausfluss ist normalerweise weiß, dick und klumpig und wird manchmal als säuerlich oder nach Essig riechend beschrieben.
Die in der Literatur am häufigsten empfohlene Behandlungsoption ist Natriumbikarbonat. Es kann als Sitzbad (z. B. Basenbad Basenbalance von Aurica) oder Vaginalspülung (z. B. Eva Douche Backpulver) verwendet werden. Während beide Optionen wahrscheinlich durch einen Puffereffekt (Erhöhung des pH-Werts) wirken, scheinen Spülungen mit einer längeren Linderung verbunden zu sein, was wahrscheinlich auf die Verringerung der vaginalen Bakterienbelastung zurückzuführen ist.
Die empfohlene Konzentration des Natriumbicarbonats beträgt 30–40 mg pro Liter Wasser. Eine Möglichkeit besteht darin, es zwei Wochen lang täglich und dann nach Bedarf zu verwenden. Die Wirkung ist tendenziell stärker, wenn die Behandlung morgens durchgeführt wird. Das Verfolgen, wann sich die Symptome entwickeln, in einem Kalender kann hilfreich sein, um vorherzusagen, wann eine Behandlung erforderlich sein wird. Hinsichtlich der Dauer der Symptome gibt es große Unterschiede. Die Aufklärung der Frauen darüber, dass die Behandlung nicht heilend ist, sondern vielmehr eine Kontrolle der Symptome ermöglicht und dass sie möglicherweise über längere Zeiträume erforderlich ist, kann zu einer besseren Akzeptanz führen.
Urethra, Skene-Drüsenöffnungen, Klitoris, Praeputium clitoridis, Frenulum, Mons pubis, Labia majora, Labia minora, Sulci interlabiales, Vestibulum, kleine Vorhofdrüsenöffnungen, Bartholini-Drüsenöffnungen, Hymen, Fourchette, Perineum, Platten-Zylinderepithel-Grenze (Linea dentata)
Verdacht auf Neoplasie:
- Macula = Kleines (<1,5 cm) farbverändertes, nicht erhabenes, nicht palpables Areal
- Fleck = Großes (>1,5 cm) farbverändertes, nicht erhabenes, nicht palpables Areal
- Papel = Kleine (<1,5 cm) erhabene und tastbare Läsion
- Plaque = Große (>1,5 cm) erhabene, palpable und abgeflachte Läsion
- Knötchen = Große Papel (>1,5 cm), öfter halbkugelförmig oder unscharf begrenzt; an der Oberfläche, innerhalb oder unter der Haut; zystische oder solide Läsion
- Zyste = Ein- bis mehrkammeriger Hohlraum, feste Kapsel; mit oder ohne Epithelauskleidung, gefüllt mit flüssigem bis festen Inhalt
- Vesikel/Bläschen = Kleine (<0,5 cm) Blase, mit klarer Flüssigkeit gefüllt
- Blase = Große (>0,5 cm) Blase, mit klarer Flüssigkeit gefüllt
- Pustel = Mit Eiter gefüllte Blase, Inhalt ist weiß oder gelb
- Hautfarben
- Rot
- Weiß
- Dunkel
Definition der Sekundärmorphologie:
(entwickelt sich aus der primären Läsion durch proliferative Umwandlung, Entzündung, Rückbildung oder Abheilung)
- Ekzem = Entzündliche, nicht infektiöse Intoleranzreaktion mit Juckreiz, unscharf begrenzte rote Plaques mit geringer Gefäßzeichnung und/oder (häufiger) Unterbrechungen der Oberfläche
- Lichenifikation = Verdickung des Gewebes mit grober kutaner Reliefstruktur, mit oder ohne Schuppung, hellrot, dunkelrot, weiß oder hautfarben
- Exkoriation = Substanzdefekt der Haut, der bis in die Dermis reicht (oft Kratzspuren)
- Purpura = Multiple, kleinfleckige Kapillarblutungen in die Haut, Unterhaut oder Schleimhaut
- Narbenbildung = Ersatzgewebe nach Wundheilung; oft weißlich, faserreich, gefäßarm
- Erosion = Flache Haut-/Schleimhaut-Veränderung mit Verlust der Epidemis/des Epithels bei intakter Dermis
- Fissur = dünner, gerader Einriss der Haut oder Schleimhaut
- Ulkus = Tiefer Substanzdefekt der Haut mit Verlust der Epidermis und Teilen der gesamten Dermis